12月1至3日,在2023年歐洲腫瘤內科學會亞洲年會(ESMO Asia)上,齊魯制藥以壁報形式報告了1類新藥艾帕洛利單抗(QL1604)單藥治療不可切除或轉移性dMMR/MSI-H實體瘤的單臂、II期關鍵臨床研究最新結果。主要研究者為復旦大學附屬腫瘤醫院郭偉劍教授和四川大學華西醫院畢鋒教授。
艾帕洛利單抗是一種與PD-1結合的高選擇性人源化單克隆抗體。研究結果顯示,艾帕洛利單抗單藥治療不可切除或轉移性dMMR/MSI-H實體瘤具有良好的療效,獨立影像評估委員會(IRRC)評估的全人群客觀緩解率(ORR)為45.8%(95%CI, 36.7-55.2),超過預設主要研究終點。
一、研究背景
DNA錯配修復缺陷(dMMR)或高度微衛星不穩定(MSI-H)是實體瘤的獨特表型[1]。DNA復制過程中,微衛星序列最易發生錯配,需要進行錯配修復,dMMR可導致移碼突變,引起微衛星不穩定(MSI)。dMMR/MSI-H實體瘤對免疫檢查點抑制劑治療反應良好,程序性死亡受體-1(PD-1)或程序性死亡配體-1(PD-L1)抑制劑治療dMMR/MSI-H實體瘤具有較高的客觀緩解率(ORR),并且緩解持續時間長[2-3]。
艾帕洛利單抗治療晚期實體瘤的I期研究表現出良好的安全性和抗腫瘤活性,在接受艾帕洛利單抗0.3-3 mg/kg Q3W的所有患者中,ORR達到20%[4]。本關鍵研究旨在評估艾帕洛利單抗單藥治療不可切除或轉移性dMMR/MSI-H實體瘤的療效和安全性。
二、研究設計和方法
本研究為單臂、II期關鍵臨床研究,納入不可切除或轉移性經組織病理學或細胞學確認的dMMR/MSI-H實體瘤患者,接受艾帕洛利單抗單藥治療,給藥方案為200mg固定劑量(如果受試者體重<40kg,給藥劑量為3mg/kg),靜脈滴注,每3周給藥1次。患者接受艾帕洛利單抗治療直至疾病進展、出現不可耐受的毒性、開始新的抗腫瘤治療、死亡、撤回知情同意等原因,最長治療時間不超過2年。治療結束后,對患者進行生存隨訪。研究的主要終點為IRRC根據實體腫瘤療效評價標準(1.1版)評估的ORR。研究設計如下圖所示。

三、研究結果
從2020年6月至2023年1月,研究共納入120例dMMR/MSI-H實體瘤患者,其中結直腸癌患者80例(66.7%),胃癌患者18例(15.0%),其它實體瘤患者22例(18.3%);97.5%的患者在入組時疾病分期為IV期,中位治療線數為2.0(范圍,0–6)。
在療效方面,截至2023年7月20日,中位隨訪時間為13.6個月,有11例患者達到完全緩解(CR),44例患者達到部分緩解(PR),ORR為45.8%(95% CI: 36.7%–55.2%),疾病控制率(DCR)為77.5%(95% CI: 69.0%–84.6%)。在結直腸癌患者中,ORR和DCR分別為42.5%(95% CI: 31.5%–54.1%)和77.5%(95% CI: 31.5%–54.1%)。中位緩解持續時間(DoR)尚未達到,6個月和12個月DoR率分別為100%和97.4%;中位無進展生存期(PFS)和中位總生存期(OS)未達到。緩解患者的靶病灶最佳變化情況如下圖所示。
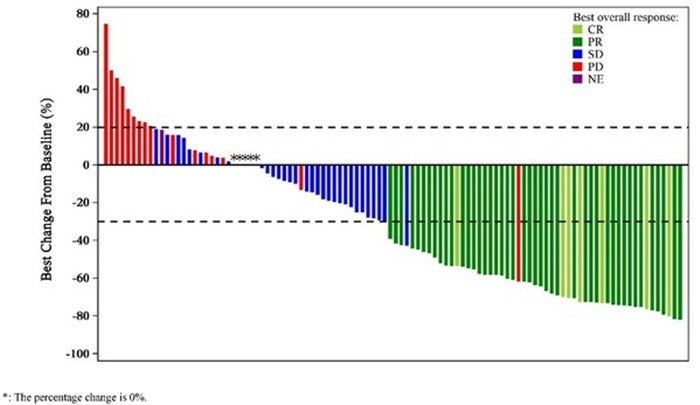
四、小結
艾帕洛利單抗單藥治療不可切除或轉移性dMMR/MSI-H實體瘤具有良好的療效和安全性。齊魯制藥艾帕洛利單抗上市申請已于今年9月獲得CDE受理。
參考文獻:
1. Bhamidipati D, Subbiah V. Tumor-agnostic drug development in dMMR/MSI-H solid tumors. Trends Cancer. 2023;9(10):828-839.
2. Le DT, et al. PD-1 Blockade in Tumors with Mismatch-Repair Deficiency. N Engl J Med. 2015;372(26):2509-20.
3. Li J, et al. Subcutaneous envafolimab monotherapy in patients with advanced defective mismatch repair/microsatellite instability high solid tumors. J Hematol Oncol. 2021;14(1):95.
4. Huang Z, et al. A first-in-human, open-label, dose-escalation and dose-expansion phase I study to evaluate the safety, tolerability, pharmacokinetics/pharmacodynamics, and antitumor activity of QL1604, a humanized anti-PD-1 mAb, in patients with advanced or metastatic solid tumors. Front Immunol. 2023;14:1258573.